上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
活性氧 Cell Meter 荧光法线粒体过氧化物检测试剂盒 适合于流式细胞仪
 |
货号 | 22970 | 存储条件 | 在零下15度以下保存, 避免光照 |
| 规格 | 100 Tests | 价格 | 3924 | |
| Ex (nm) | 540 | Em (nm) | 590 | |
| 分子量 | 溶剂 | |||
| 产品详细介绍 | ||||
简要概述
线粒体是细胞超氧化物的主要生产者。低中等水平的超氧化物的产生对于许多重要细胞过程的适当调节至关重要,这些过程包括基因表达,信号转导和肌肉对耐力运动训练的适应性。不受控制的线粒体超氧化物的产生会触发细胞氧化损伤,从而导致多种疾病的发病机理,包括癌症,心血管疾病,神经退行性疾病和衰老。Cell Meter 荧光法线粒体过氧化物检测试剂盒使用我们独特的超氧化物指示剂来定量活细胞中的超氧化物水平。MitoROS 580具有活细胞渗透性,可以快速,选择性地靶向线粒体中的超氧化物。与超氧化物反应时会生成红色荧光。Cell Meter 荧光法线粒体过氧化物检测试剂盒提供了一种灵敏的一步荧光测定法,可在培养一小时后检测活细胞中的线粒体超氧化物。该试剂盒针对流式细胞仪应用进行了优化。金畔生物是AAT Bioquest的中国代理商,为您提供最优质的Cell Meter 荧光法线粒体过氧化物检测试剂盒。
活性氧(ROS)篇:包含总ROS和多种活性氧离子检测试剂大全
适用仪器
| 流式细胞仪 | |
| 激发: | 488nm激光 |
| 发射: | 575/26nm滤波片 |
| 通道: | PE通道 |
产品说明书
样品实验方案
简要概述
- 准备细胞密度为0.5-1×10 6细胞/ mL
- 用测试化合物处理细胞以诱导超氧化物
- 将1 µL 500X MitoROS 580加到0.5 mL细胞悬液中
- 将细胞在37°C染色1小时
- 使用带有FL2通道的流式细胞仪检测荧光强度
溶液配制
储备溶液配制
1. MitoROS 580储备溶液(500X):将100 µL DMSO(组分C)添加到MitoROS 580(组分A)小瓶中,并充分混合以制成500X MitoROS 580储备溶液。避光。注意:请密闭存放。
实验步骤
- 对于每个样品,在自备的0.5 mL生长培养基或缓冲液中制备细胞,密度为5×10 5至1×10 6个细胞/ mL。注意:应单独评估每种细胞系,以确定超氧化物诱导的最佳细胞密度。
- 在分析缓冲液(组分B)或自备的缓冲液(例如PBS)中用25 µL 20X测试化合物处理细胞以诱导超氧化物。对于对照细胞(未处理的细胞),添加相应量的化合物缓冲液。
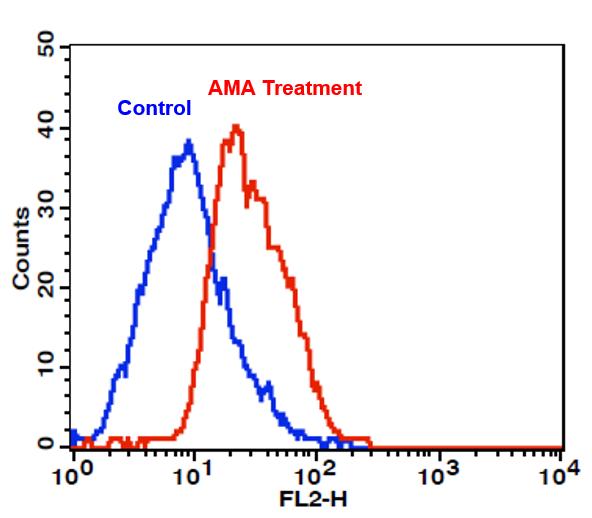
- 将细胞在37°C孵育至少30分钟。注意:将 Jurkat细胞在37°C下用50 µM抗霉素A(AMA)处理30分钟以诱导超氧化物。有关详细信息,请参见图1。
- 将0.5 µL细胞悬浮液中加入1 µL 500X MitoROS 580储备液。
- 在37°C下孵育1小时。注意:对于贴壁细胞,用0.5 mM EDTA轻轻提起细胞以保持细胞完整,并在MitoROS 580孵育之前用含血清的培养基洗涤一次。适当的孵育时间取决于单个细胞的类型和测试使用的化合物。
- 使用带有FL2通道的流式细胞仪(Ex / Em = 488/590 nm)检测荧光强度。
图示
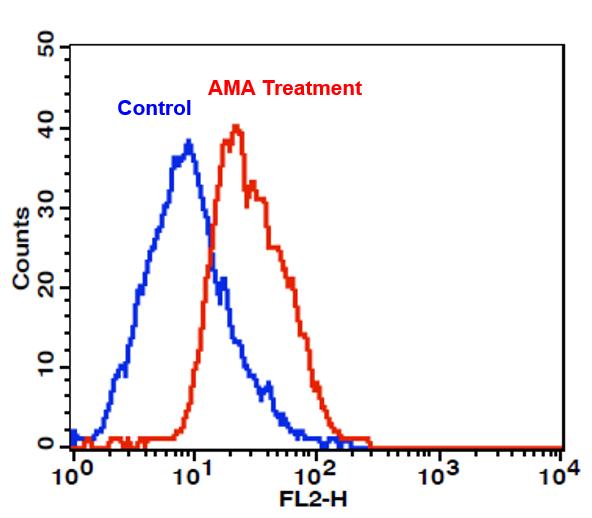 图1.使用Cell Meter 荧光细胞内超氧化物检测试剂盒检测Jurkat细胞中的超氧化物。AMA处理(红色):将细胞在37°C下用50 µM抗霉素A(AMA)处理30分钟,然后与MitoROS 580孵育1小时。对照(蓝色):在未经AMA处理的情况下,将细胞与MitoROS 580在37°C孵育1小时。使用流式细胞仪(BD FACSCalibur)在FL2通道检测上荧光信号。 |
参考文献
Concentration-dependent effect of sodium hypochlorite on stem cells of apical papilla survival and differentiation
Authors: Martin DE, De Almeida JF, Henry MA, Khaing ZZ, Schmidt CE, Teixeira FB, Diogenes A.
Journal: J Endod (2014): 51
Effect of hypochlorite oxidation on cholinesterase-inhibition assay of acetonitrile extracts from fruits and vegetables for monitoring traces of organophosphate pesticides
Authors: Kitamura K, Maruyama K, Hamano S, Kishi T, Kawakami T, Takahashi Y, Onodera S.
Journal: J Toxicol Sci (2014): 71
A simple yet effective chromogenic reagent for the rapid estimation of bromate and hypochlorite in drinking water
Authors: Zhang J, Yang X.
Journal: Analyst (2013): 434
Analysis of the germination kinetics of individual Bacillus subtilis spores treated with hydrogen peroxide or sodium hypochlorite
Authors: Setlow B, Yu J, Li YQ, Setlow P.
Journal: Lett Appl Microbiol (2013): 259
Comparative antimicrobial activities of aerosolized sodium hypochlorite, chlorine dioxide, and electrochemically activated solutions evaluated using a novel standardized assay
Authors: Thorn RM, Robinson GM, Reynolds DM.
Journal: Antimicrob Agents Chemother (2013): 2216
Effect of hypochlorite-based disinfectants on inactivation of murine norovirus and attempt to eliminate or prevent infection in mice by addition to drinking water
Authors: Takimoto K, Taharaguchi M, Sakai K, Takagi H, Tohya Y, Yamada YK.
Journal: Exp Anim (2013): 237
Green synthesis of carbon dots with down- and up-conversion fluorescent properties for sensitive detection of hypochlorite with a dual-readout assay
Authors: Yin B, Deng J, Peng X, Long Q, Zhao J, Lu Q, Chen Q, Li H, Tang H, Zhang Y, Yao S.
Journal: Analyst (2013): 6551
Use of pyrogallol red and pyranine as probes to evaluate antioxidant capacities towards hypochlorite
Authors: Perez-Cruz F, Cortes C, Atala E, Bohle P, Valenzuela F, Olea-Azar C, Speisky H, Aspee A, Lissi E, Lopez-Alarcon C, Bridi R.
Journal: Molecules (2013): 1638
A novel flow-injection analysis system for evaluation of antioxidants by using sodium dichloroisocyanurate as a source of hypochlorite anion
Authors: Ichiba H, Hanami K, Yagasaki K, Tanaka M, Ito H, Fukushima T.
Journal: Drug Discov Ther (2012): 44
Colorimetric determination of hypochlorite with unmodified gold nanoparticles through the oxidation of a stabilizer thiol compound
Authors: Zhang J, Wang X, Yang X.
Journal: Analyst (2012): 2806
